事業内容Business
- HOME
- 事業内容
プラットフォーム・技術
ヒト呼吸器官への高い感染親和性を有するヒトパラインフルエンザウイルスを用いたプラットフォーム型ベクターシステムを構築しました。当該ベクターを用いて感染症対応ワクチン及び腫瘍特異的な抗腫瘍免疫剤の開発を行っております。
ベクター技術BC-PIVベクター(主要技術)
バイオコモ株式会社(BioComo Inc.)は、ヒトパラインフルエンザウイルス2型(hPIV2)を基に、
ウイルス膜タンパク質を構成する遺伝子の一部を欠損した非伝播型のウイルスベクターを三重大学と
共同で開発し、BC-PIV(社名とウイルス(hPIV)に因み)と命名しました。
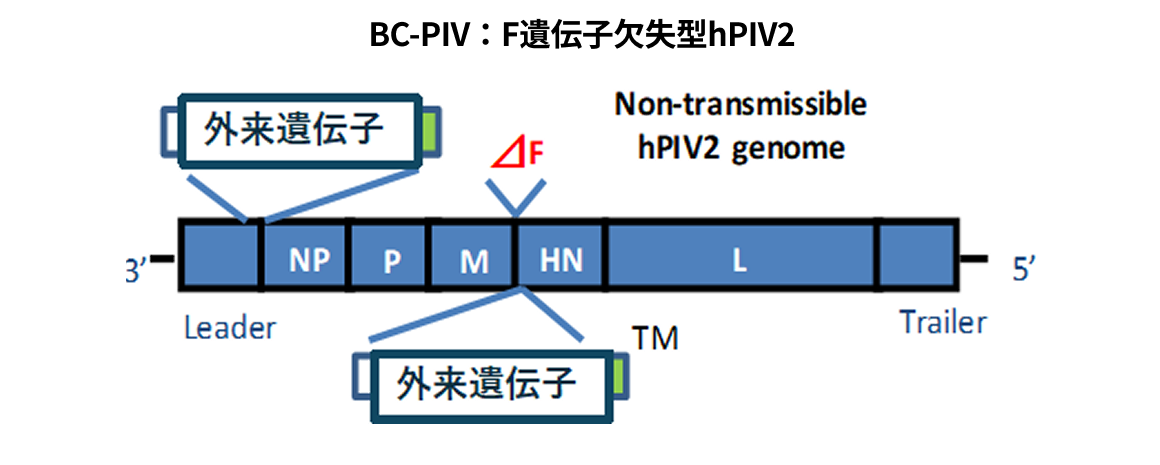
BC-PIVベクターとは
BC-PIVベクターは、ベクター紹介説明図にあるようにウイルスゲノム上からF膜タンパク質遺伝子を欠失している(BC-PIV感染にはウイルス粒子上に存在する2種類のHN膜タンパク質及び F膜タンパク質が必須 説明図 項目1)ため、通常の細胞感染では2次感染性ウイルス粒子*1が産生されません。そのため、通常の細胞・組織に感染したBC-PIVベクターは2次感染性ウイルスが増殖せず、感染した細胞以外に広がることがないため高い安全性が担保されます。一方、1次感染性ウイルス粒子*2作製のため、ウイルスゲノムから欠失したF膜タンパク質を発現(供給)する組換え細胞を作製しました。当該細胞を用いることにより、F膜タンパク質を取り込んだ1次感染性能を有する高力価BC-PIVベクターを作製することが可能となります(説明図 項目2)。樹立した組換え細胞は、特許により権利を確保しており、ICHガイドライン*3に則ったマスターセルバンク(MCB*4)として保管されてGMP*5でベクターの製造が可能な状態です。
- *1 2次感染性ウイルス粒子:1次感染性ウイルス粒子が感染した細胞内で新たに作られたウイルスが細胞に感染することできるウイルス
- *2 1次感染性ウイルス粒子:最初に細胞に感染するウイルス
- *3 ICHガイドライン:医薬品の品質・安全性・有効性に関する国際的な統一基準
- *4 MCB(Master Cell Bank):医薬品製造の基準を満たした細胞基材
- *5 GMP(Good Manufacturing Practice):医薬品の品質を担保するための製造管理と品質管理の基準
BC-PIVの特性
外来遺伝子導入と発現
BC-PIVベクターには最大3種類の遺伝子を同時に導入することができます。
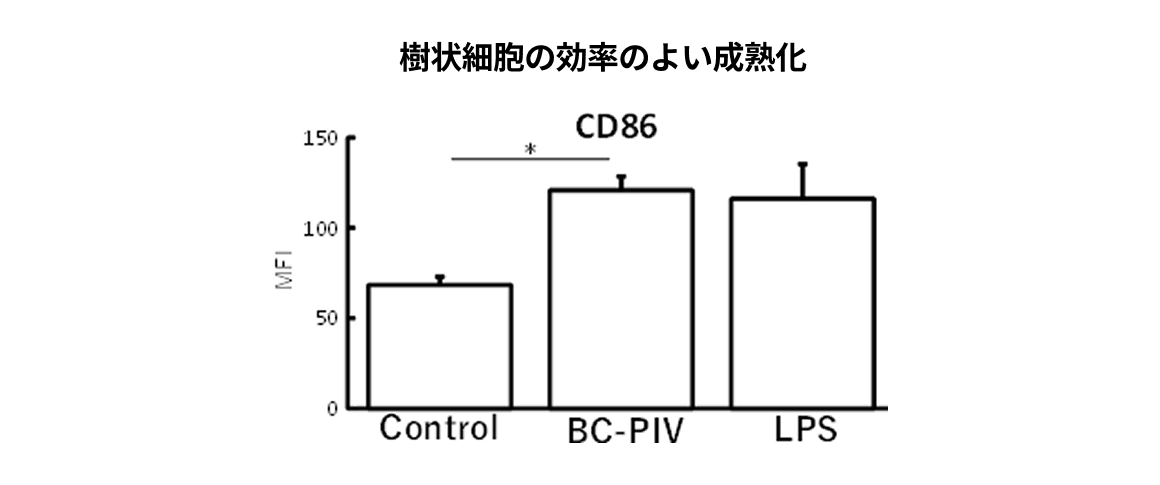
また、BC-PIVベクター感染細胞・組織での導入遺伝子の発現も高く、レトロウイルスの100倍以上のタンパク質発現を確認しております。さらに、樹状細胞へも効率的に感染し(説明図 項目4)、免疫活性の指標となるCD86等の共刺激物質を強く誘導します。それに伴い突起伸長を伴う樹状細胞を成熟化させることができ、抗原提示細胞の効率的活性化をもたらします。
ベクター表面に導入タンパク質の提示が可能
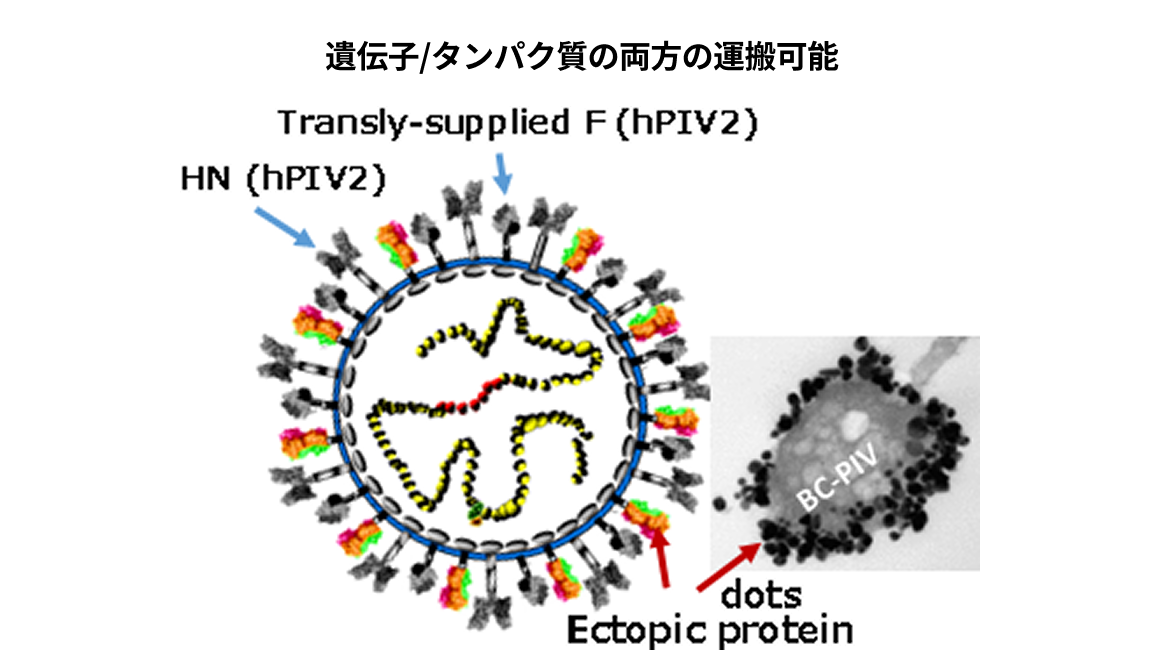
BC-PIVベクターに導入した外来遺伝子がコードするタンパク質を、感染細胞で発現させるだけでなく、ベクター表面に停留可能なアンカーシグナルなどを付加することにより、ベクター粒子上に当該タンパク質を搭載させることが可能です。必要であれは当該タンパク質の立体構造を維持でき、また多量体を形成させることも可能です(説明図 項目5)。
繰り返し投与が可能
BC-PIVベクターに対する中和抗体誘導能は高くなく、繰し返し投与が可能です。特に、経鼻投与では繰り返し投与の効果が確認されています(説明図 項目6)。
ベクター作製が短期間で容易
ベクター作製技術の改良により、最短で外来遺伝子導入したBC-PIVベクター作製が3週間程度で可能です(説明図 項目7)。
BC-PIVプラットホームベクター技術
(ヒトパラインフルエンザウイルス2型由来)説明図
- 非増殖特性による高い安全性及び複数の遺伝子を導入可能
- ゲノムからF膜遺伝子を欠失し、2次感染性粒子を産生せず高い安全性特性を保持
- 外来遺伝子は同時に3種類導入可能
- 高力価ベクター産生細胞(MCB)
- トランスにF膜タンパク質を提供し、高力価のBC-PIVを産生する組換え細胞を樹立
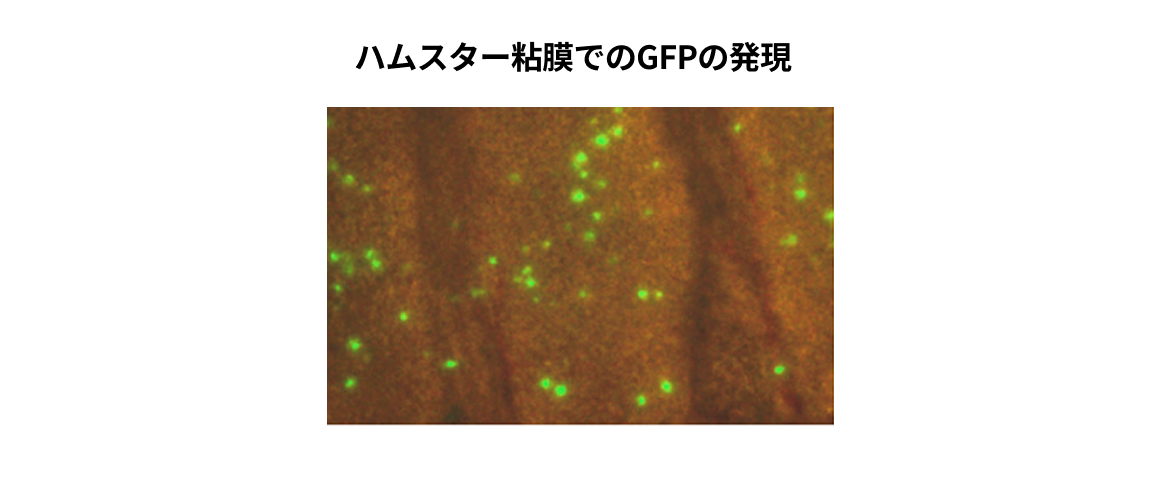
- 経鼻投与で強い粘膜IgAと血清IgGを誘導
- BC-PIVベクター(hPIV2)の特性で粘膜上皮等に感染し遺伝子を発現
- 筋肉投与、皮内投与、腫瘍内投与も可能
- 樹状細胞の効率のよい成熟化
- 抗原遺伝子/タンパク質の運搬による強い免疫反応誘導
- BC-PIVベクターは、抗原遺伝子だけでなく天然構造を有する抗原をベクター表面に提示
- 繰り返し投与が可能
- 特に、経鼻では何回も繰り返し投与可能:動物試験で確認済
- 短期間(3週間程度)で新規BC-PIVの回収可能
- 効率的なリバースジェネティクス法を確立
開発パイプライン
BC-PIVベクターを用いた感染症ワクチンを提供する場合、対象感染症の最適化抗原タンパク質を産生する遺伝子をBC-PIVベクターに導入し、経鼻ワクチンとして利用可能です。一方、がんの場合、腫瘍内に効率的に免疫細胞を誘導できるようなサイトカイン、ケモカイン等の複数の遺伝子を導入したBC-PIVを投与することによる難治性がんに対する新規治療法の開発を目指しています。
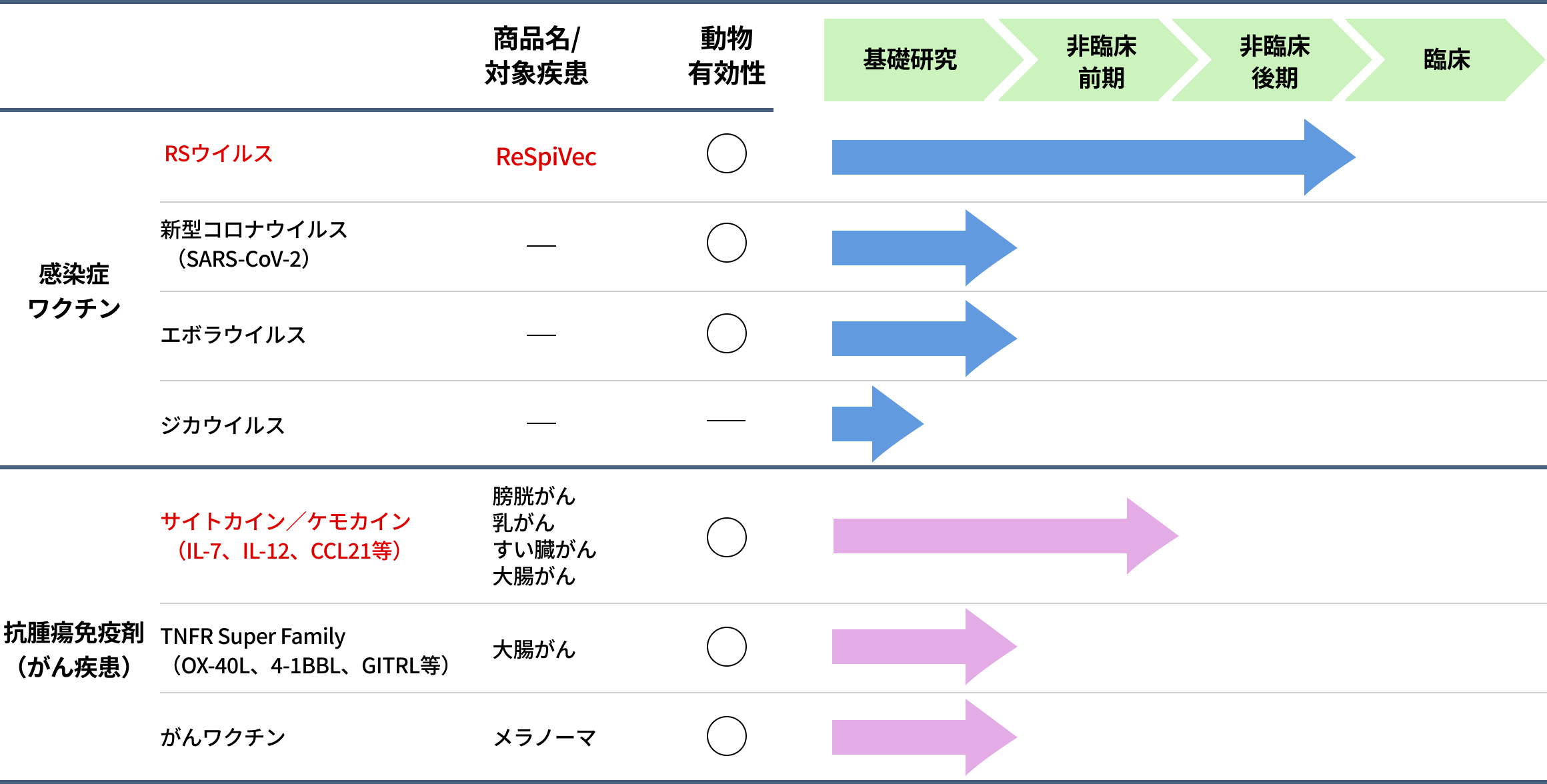
感染症ワクチン
RSVワクチン
RSウイルス(RSV)はヒトの呼吸器に感染するウイルスで、生涯を通じて繰り返し感染が起こります。健康成人では通常、軽い感冒(風邪)症状で済むことが多いですが、初めて感染する乳幼児及び免疫が弱くなっている高齢者では、気管支炎、細気管支炎、肺炎などが重症化することが知られています。RSVワクチン開発は50年以上続けられており、2023年にようやく高齢者向けのワクチンが認可され、RSVに対する高い効果が示されています。高齢者向けRSVワクチンはブロックバスター*6となり、RSVワクチンは大きな市場となっています。
一方、乳幼児には有効なRSVワクチンは未だ認可されていません。これは大人とは異なり乳幼児の免疫が未熟であることに起因しており、乳幼児向けのRSVワクチンの開発が難しいことを物語っております。
我々は、NIH(アメリカ国立衛生研究所)で開発されたRSVのF膜タンパク質の抗原としての利用価値を高めた安定的変異体タンパク質(DS-Cav1*7)の使用ライセンスを受け、経鼻ワクチンBC-PIV/DS-Cav1 (商品名:ReSpiVec)を開発しております。同じパラミクソウイルス科でBC-PIVベクターとは異なる型のパラインフルエンザウイルスを用いたRSV野生型抗原ワクチンでは、乳幼児での臨床試験でRSV感染防御効果が報告されており、ReSpiVecも高齢者だけでなく、乳幼児向けワクチンとして開発を進めております*7。
ハムスターにReSpiVecを経鼻投与した結果、高い抗RSV F抗体を誘導し、またRSVの感染・増殖抑制も認められたため、ヒトにおいてもReSpiVecのワクチン効果が期待されます。
ReSpiVecの開発は、AMEDに設置されている先進的研究開発戦略センター(SCARDA)の「新規モダリティを用いる感染症ワクチンの研究開発_1」で国立大学法人 三重大学の野阪哲哉教授を研究開発代表者とする、研究課題名「新規細胞質型RNAウイルスベクターを用いた新興・再興感染症ワクチン作製プラットフォームの確立と遺伝子組換えワクチンのカタログ化」のプロジェクトとして助成を受け、現在、非臨床から臨床への開発を進めております。
- *6 ブロックバスター:世界で年間1000億円以上売り上げる医薬品
- *7 DS-Cav1:効率よく中和抗体が誘導できる“不安定状態を維持”RSV F膜タンパク質抗原。これにより“安定状態優勢”な野生型タンパク質抗原より高い中和抗体の誘導が期待できる。
コロナウイルスワクチン(COVID-19)
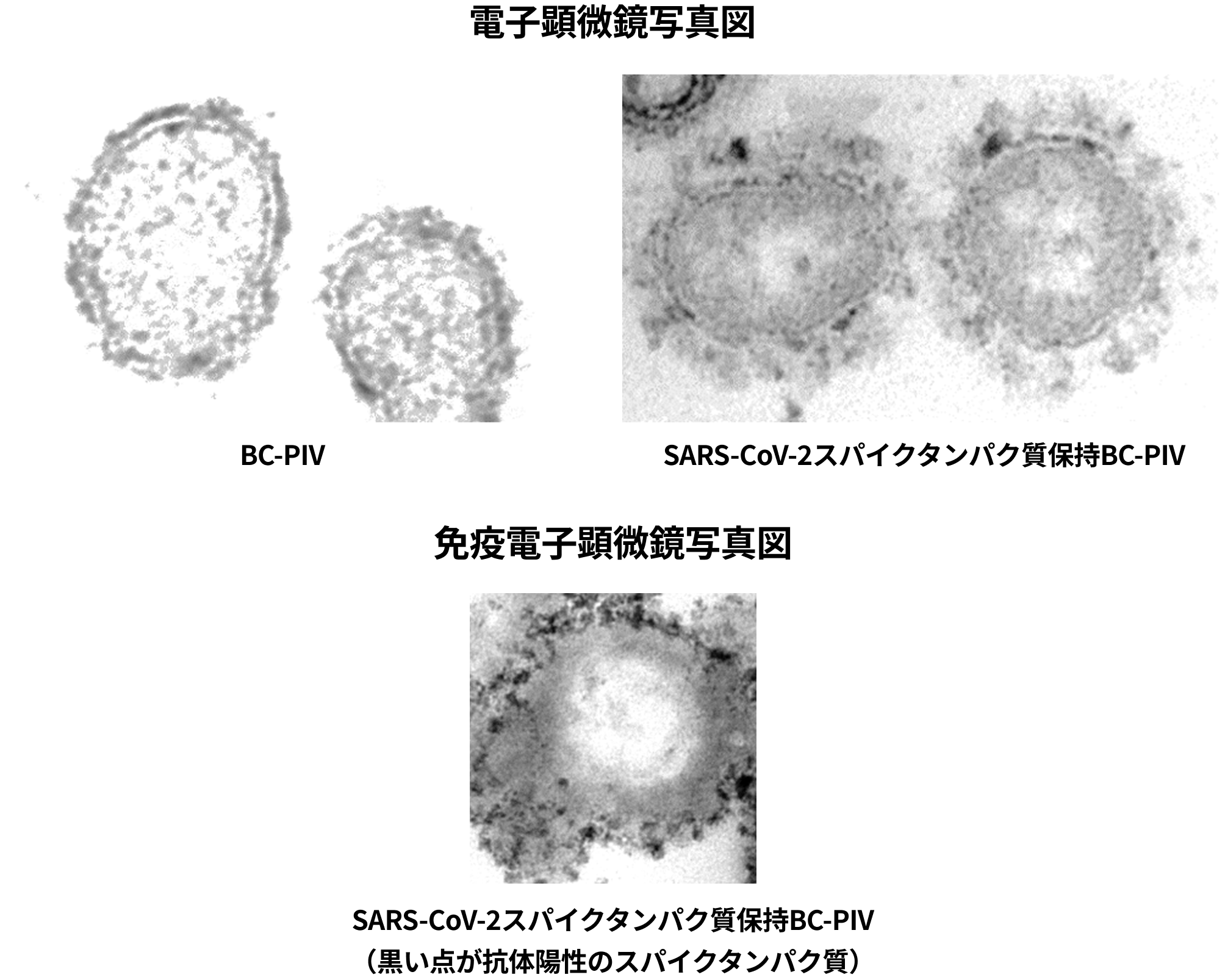
武漢株、アルファ株(B.1.1.7)、ベータ株(B.1.351)、ガンマ株(P.1)、デルタ株 (B.1.617.2)、カッパ株(B.1.617.1)、ラムダ株(C.37)、ミュー株(B.1.621)、オミクロン株(B.1.1.529、BA.1、BA.2)のRBD*8領域を含む各株のスパイクタンパク質遺伝子を導入したワクチン(BC-PIV/S2PM)を作製しました。当該ワクチンではSARS-CoV-2の高分子量スパイクタンパク質をBC-PIVベクター粒子上に3量体で提示する形態で導入しました。電子顕微鏡写真図で示すように、SARS-CoV-2のスパイクタンパク質を導入したBC-PIVベクターでは、ベクター表面上に大きなスパイクタンパク質が確認でき、さらにこれを抗スパイクタンパク質抗体を用いた免疫電子顕微鏡写真図で確認すると、ベクター表面上に多くの抗体陽性のスパイクタンパク質が認められ、前述の大きなスパイクタンパク質がSARS-CoV-2のスパイクタンパク質であることが確認できます。
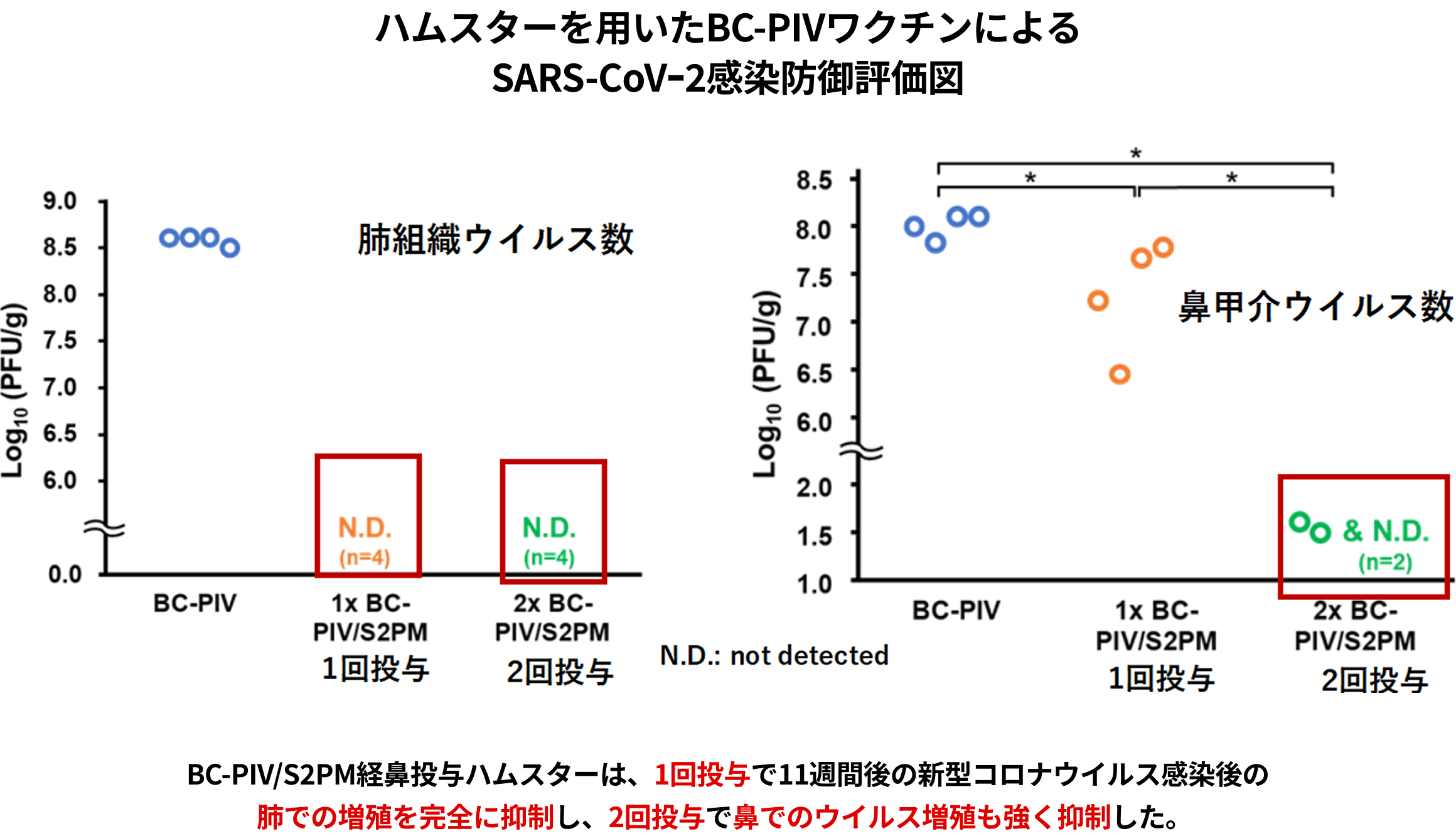
当該ワクチンにおけるコロナウイルスの感染防御効果は、ハムスターに当該ワクチンを1回又は2回経鼻投与した後、コロナウイルスに感染させて確認しました。1回投与でも肺のコロナウイルス増殖は完全に抑制されており、2回投与では肺だけではなく、さらに鼻腔でのコロナウイルス増殖も抑制されていたため、この結果より当該ワクチンの高い感染防御効果が認められました(ハムスターを用いたBC-PIVワクチンによるSARS-CoV-2感染防御評価図)。
- *8 RBD(Recepter Binding Domain):スパイクタンパク質の受容体結合部位
抗腫瘍免疫剤
我々は以下のテーマを掲げ、抗腫瘍免疫剤の開発を進めております。
- 樹状細胞(DC)活性化による細胞傷害性Tリンパ球(CTL)を中心とする免疫細胞の効率的誘導
- 腫瘍浸潤性リンパ球(TIL)の腫瘍内への効率的な浸潤誘導
- 腫瘍内に三次リンパ様構造(TLS)免疫群の誘導
- 腫瘍内のM2→M1マクロファージへの転換
- Cold cancerへの対応
ColdからHotへの転換
CAF (Cancer Associated Fibroblast(myCAF、iCAF、老化CAF等))への対応 - がんワクチンによる対応
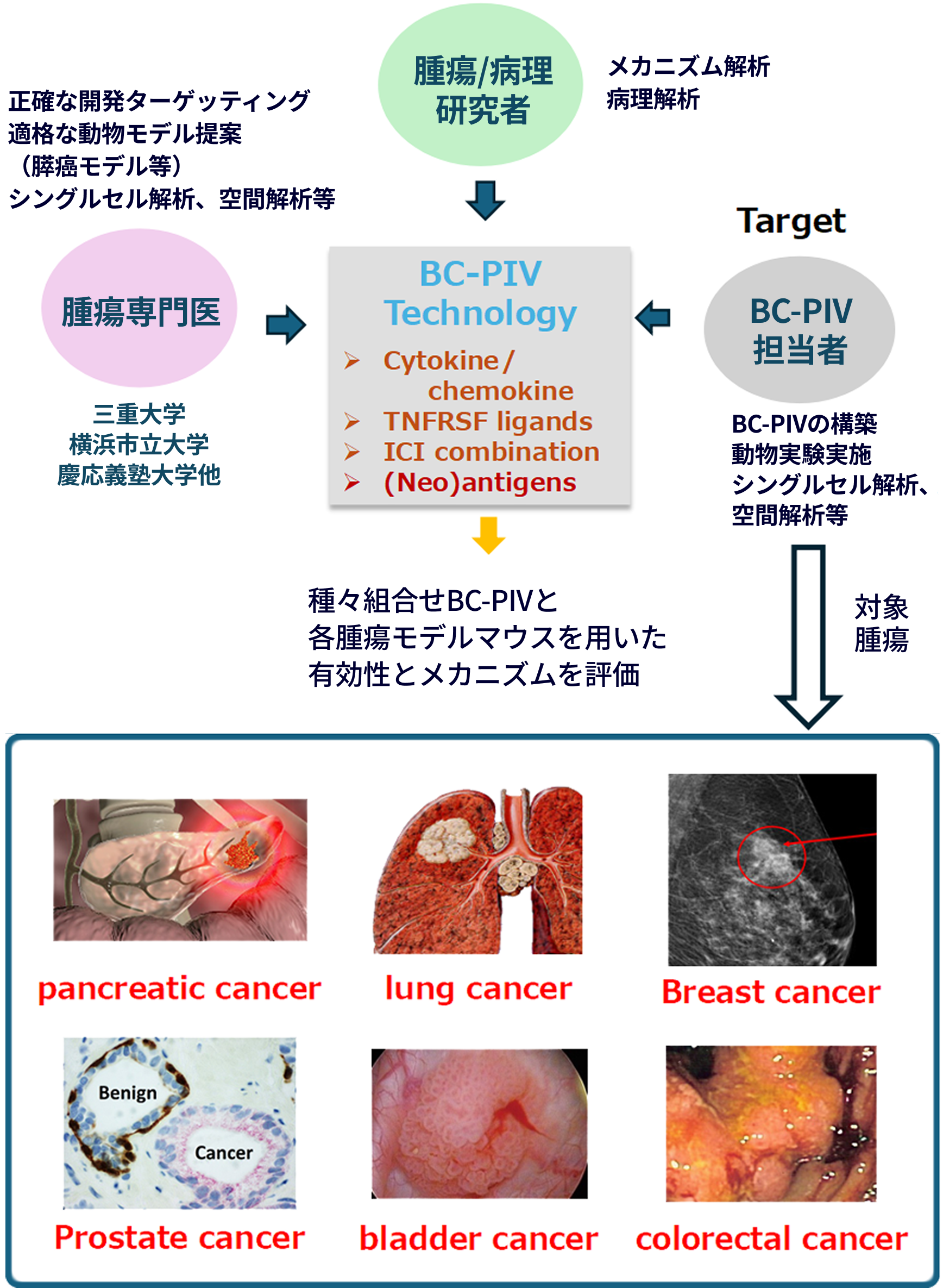
上記に対応した様々な遺伝子又は遺伝子/タンパク質を提示するBC-PIVベクターを構築し、各腫瘍に対する抗腫瘍免疫剤の開発を進めております。
具体的には以下に示す遺伝子を、単独又は2種類、3種類を組み合わせ、BC-PIVベクターに導入しております。
- サイトカイン:IL-2、 IL-7、 IL-12、 IL-15、 GM-CSF等
- ケモカイン:CCL19、CCL21等
- TNFα受容体関連リガンド:
OX40リガンド、4-1BBリガンド、 GITRリガンド
CD27リガンド、 CD30リガンド - 抗体:scFv等
- ネオアンチゲン:各種抗原ペプチド
- その他関連遺伝子
試験例
(1)OX40受容体、4-1BB受容体のようなTNF受容体スーパーファミリー(TNFRSF)分子群は活性化T細胞等の表面上に誘導的(一時的)に発現します。一方、活性化樹状細胞では、OX40リガンド 、4-1BBリガンド等のリガンドを発現します。T細胞は抗原とリガンドによりシグナル1*9及びシグナル2*10を受け取る事で活性化され、がん細胞を攻撃するエフェクターT細胞に分化します。 過去に、強いリガンド作用をもつアゴニスト抗体を用いた治験が実施されましたが、天然型リガンドでないアゴニスト抗体はリガンド/受容体より結合作用が強くT細胞に過剰な刺激となり、その結果、肝臓の重篤な副作用が発生したため治験が取りやめになった経緯があります。そこで、我々は天然型のTNFRSFリガンドをBC-PIVベクター上に発現させる事で、自然なT細胞の活性化により抗腫瘍免疫が成立するとの仮説を立て、実際にシグナル1及びシグナル2を活性化させて、肝臓での副作用を起こすことなく抗腫瘍効果が得られる事を、動物試験で確認いたしました。
- *9 シグナル1:T細胞レセプター(TCR)によってT細胞内に伝達する抗原特異的なシグナル⇒BC-PIVベクターはウイルスベクターであり、腫瘍に投与したBC-PIVベクターの作用と樹状細胞の成熟化作用によりシグナル1に寄与すると考えています。
- *10 シグナル2:抗原特異性のない補助シグナル⇒OX40リガンド、 4-1BBリガンド、 GITRリガンド、 CD27リガンド、 CD30リガンドをコードする遺伝子をBC-PIVベクターに導入し、これら3量体リガンドタンパク質はベクター粒子表面上に提示され、T細胞のシグナル2次刺激を促進します。
マウス大腸がんCT-26に対する効果
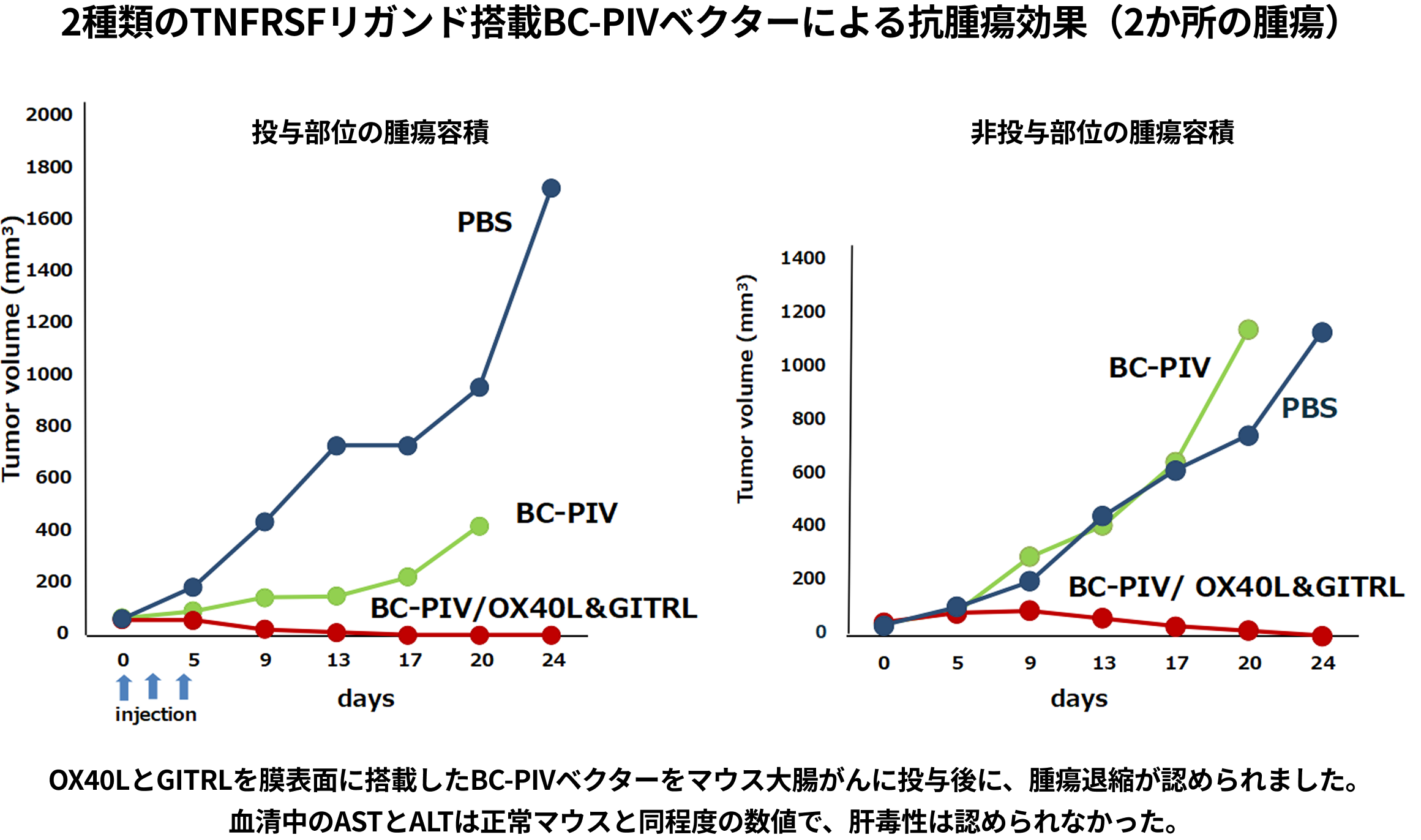
マウス大腸がん(CT-26細胞)に対して、OX40リガンドとGITRリガンドを粒子表面上に保持するBC-PIVを投与すると、投与巣だけでなく非投与巣のがん細胞も消失しました(2種類TNFRSFリガンド搭載BC-PIVによる抗腫瘍効果を示す図)。さらに当該マウスは、がん細胞が消失して約8カ月が経過してもCT-26細胞に対するCTLを維持していることが確認されています。この際、マウス肝臓での肝毒性は認められませんでした。
これらの結果より、OX40リガンドとGITRリガンドを保持するBC-PIVを投与することにより抗腫瘍免疫が立ち上がり腫瘍を排除、非投与側の腫瘍も排除し、マウスでは強いアブスコパル効果*11があることも推察されました。
- *11 アブスコパル効果:治療したがん細胞に対して効果的に機能する抗腫瘍免疫が、転移した同じがん細胞に対しても抗腫瘍免疫の効果がみられること
(2)サイトカインとケモカインによる効果
サイトカインとケモカインを導入したBC-PIVベクターによりマウスのHot又はColdな腫瘍に対して極めて高い抗腫瘍効果が確認されております。
抗腫瘍免疫剤開発コンソーシアムチームの立ち上げ
抗腫瘍免疫剤開発に関して、ベクター開発及び免疫関連の基礎研究者だけでは、臨床でのがんの治療には向かない開発を行うことになりがちです。我々は、無駄な開発を避け、より早いBC-PIV抗腫瘍ベクターを提供するため、臨床の先生方を含め、最近のホットなArea of Interestな情報を基に抗腫瘍免疫剤の開発進めることができるよう、様々な分野の医師や研究者などで構成されたコンソーシアムを2024年に立ち上げました。特に、最先端で抗がん剤等の臨床開発に携わっておられる臨床の先生方と共同開発を行うことにより、的確な開発の認識と情報のup dateに努めて開発を進めてまいります。